Alkane, Laserblitze und BESSYs Röntgenblick
Einem internationalen Forschungsteam ist es gelungen, einen Zwischenschritt bei der Katalyse von Alkanen zu beobachten
Einem internationalen Forschungsteam ist es gelungen, einen Zwischenschritt bei der Katalyse von Alkanen zu beobachten. Mit dem Verständnis dieser Reaktionen lassen sich in Zukunft bestehende Katalysatoren optimieren und neue finden, um zum Beispiel das Treibhausgas Methan in wertvolle Grundstoffe für die Industrie zu verwandeln.
Unsere Beziehung zum Methan ist zwiegespalten. Einerseits ist das leichteste Alkan ein hochpotentes Klimagas. Es heizt den Treibhauseffekt gut 28-mal stärker an als Kohlendioxid. Andererseits ist es aber auch ein interessanter Rohstoff. Nicht nur, um ihn in einer Gasheizung zu verbrennen. Denn ist die C-H-Bindung, also jene zwischen Kohlenstoff- und Wasserstoffatomen, erst einmal geknackt, lassen sich aus dem Treibhausgas verschiedenste Grundstoffe für die Industrie herstellen.
Klingt eigentlich nach einer guten Lösung. Doch eben jene Bindung im Methan stellt Chemikern schon seit Jahrzehnten vor eine große Herausforderung: Sie ist eine der stärksten Bindungen in der Natur. Mit Katalysatoren gelingt es zwar schon länger, sie zu brechen. Wie das im Detail funktioniert, ist bis heute aber unklar.
Nun war ein internationales Forschungsteam unter Leitung von Wissenschaftler*innen der Universität Uppsala zusammen mit Kolleginnen und Kollegen der Universitäten Hamburg und Stockholm, des Max-Born-Instituts und des Helmholtz-Zentrum Berlin bei Zwischenstufen dieser Katalyse live dabei.
Schnappschüsse vom Sigma-Komplex
„Vor über fünfzig Jahren haben Forscher festgestellt, dass die C-H-Bindungen aufbrechen, wenn man spezielle Metallkatalysatoren hinzufügt und sie dann mit sichtbarem Licht bestrahlt“, erklärt der leitende Experimentator der Studie Raphael Jay von der Universität Uppsala. „Was dabei genau passiert, wie sich also die Alkanmoleküle den Metallkatalysatoren nähern und an ihnen hängen bleiben, war bis heute ein Rätsel.“
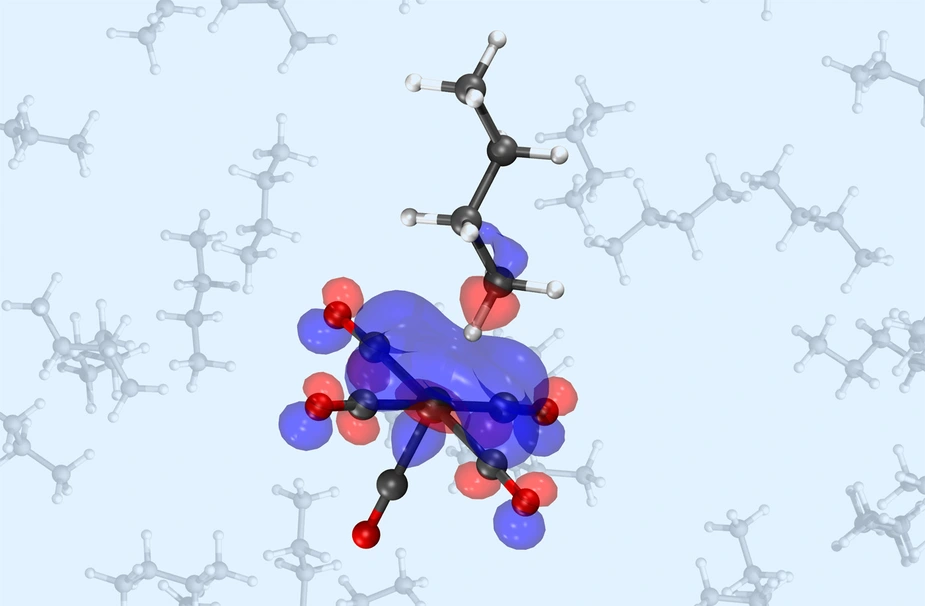
Dieses wollten die Forschungsteams lösen. Als Katalysator wählten sie Chromhexacarbonyl, ein hochsymmetrisches, gesättigtes und unreaktives System mit einem Chromatom im Zentrum. Das führt zwar nicht zur kompletten Aufspaltung der Alkane, aber zu einem wichtigen Zwischenschritt der Reaktion – der Bildung des Sigma-Komplexes. „Mit einem UV-Puls spalten wir eine Carbonylgruppe ab, sodass eine Art Öffnung entsteht“, erklärt Raphael Jay. „Das Metall wird hochreaktiv, will unbedingt etwas binden und fängt deshalb eine C-H-Gruppe ein. Die dockt als Ganzes an das Metallatom an. Das nennen wir den Sigma-Komplex.“
Die einzelnen Schritte vom Anknipsen des Lichtes bis zum fertigen Komplex haben er und sein Team im Laserlabor der Huse-Gruppe an der Universität Hamburg beobachtet. Mit optischen Lichtpulsen nahmen sie die Reaktion in ultrakurzen Schnappschüssen auf. Die zeigten, dass der Katalysator bereits nach weniger als 100 Femtosekunden aktiviert war. Das ist so kurz, dass selbst das Licht in dieser Zeit nur drei Hundertstel eines Millimeters vorankommt. Er wird dabei sehr heiß und seine Bestandteile schwingen um das Chromatom. Erst wenn die Schwingungen aufhören, kann sich das Alkan dem Katalysator nähern und den Sigma-Komplex bilden. Das geschieht in acht Pikosekunden – einer Zeitspanne, in der das Licht rund 2,4 Millimeter zurücklegt.
Röntgenstrahl und Flüssigkeitsscheibchen
„Mit der optischen Spektroskopie haben wir also die Schritte zum Sigma-Komplex nachverfolgt“, erzählt Raphael Jay. „Die entstandenen Bindungen wollten wir dann mit Röntgenstrahlen charakterisieren.“ Dazu kamen sie für ein weiteres Experiment ans HZB nach Berlin. Denn die Beamline UE52-SGM mit der Endstation AXSYS-NEXAFS BESSY II sei dafür einfach prädestiniert, meint der Physiker, der an dieser bereits für seine Dissertation forschte. „Mir ist kein anderes Synchrotron auf der Welt bekannt, wo es einen solchen Aufbau gibt, wie wir ihn gewählt haben“, sagt er.
Und tatsächlich hat es das Experiment in sich. Zuerst wählten die Forscher längerkettige Alkane, da diese im Gegensatz zu Methan unter normalen Umgebungsbedingungen flüssig sind. Das macht die Untersuchung mit dem Röntgenstrahl einfacher. Allerdings werden weiche Röntgenstrahlen vom Kohlenstoff in den Alkanen absorbiert. Die Lösung bestand aus zwei schräg nebeneinanderliegenden Düsen, die die Alkane mit dem Katalysator in die Experimentierkammer spritzten. „Wenn die beiden Flüssigkeitsstrahlen im Vakuum kollidieren, bilden sie eine hauchdünne Flüssigkeitsscheibe“, erklärt Mattis Fondell vom HZB-Institut Methoden und Instrumentierung der Forschung mit Synchrotronstrahlung, der den Aufbau des Experiments entwickelt hat. „Diese ist dünn genug, dass sie das weiche Röntgenlicht nicht vollständig absorbiert. Anhand der Stärke der Absorption für unterschiedliche Wellenlängen des Röntgenlichts können wir uns gezielt bestimmte chemische Bindungen in den Molekülen ansehen.“ Auf diese Weise tasteten die Forschenden den Sigma-Komplex in der Flüssigkeit mit hoher Empfindlichkeit ab und hielten fest, auf welche Weise sich die Bindung zwischen Metall und Alkan bildet.
„Als Nächstes wollen wir verstehen, wie die Struktur des Katalysators und das Metall in seinem Zentrum die Art und Weise beeinflussen, wie er angeschaltet wird und wie er mit Alkanen interagiert“, gibt Raphael Jay einen Ausblick. „Dies wird es ermöglichen, sein Verhalten bei Aktivierungsreaktionen von C-H-Bindungen besser zu steuern und anzupassen.“
Publikation:
Photochemical Formation and Electronic Structure of an Alkane σ-Complex from Time-Resolved Optical and X-ray Absorption Spectroscopy
Raphael M. Jay, Michael R. Coates, Huan Zhao, Marc-Oliver Winghart, Peng Han, Ru-Pan Wang, Jessica Harich, Ambar Banerjee, Hampus Wikmark, Mattis Fondell, Erik T. J. Nibbering, Michael Odelius, Nils Huse, and Philippe Wernet
Journal of the American Chemical Society 2024146 (20), 14000-14011. DOI: 10.1021/jacs.4c02077
Kontakt:
Helmholtz-Zentrum Berlin für Materialien und Energie
Institut Methoden und Instrumentierung der Forschung mit Synchrotronstrahlung
Dr. Lars Birger Mattis Fondell
+49 30 8062-13448
mattis.fondell(at)helmholtz-berlin.de
Dr. rer. nat. Sebastian Eckert / TU Berlin
+49 30 8062-14465
sebastian.eckert(at)helmholtz-berlin.de
Pressemitteilung HZB vom 31.05.2024