Wasser lässt das Proton zittern
MBI-Forscher beschreiben ultraschnelle Bewegungen und kurzlebige Strukturen hydratisierter Protonen
Protonen in wässriger Umgebung spielen eine Schlüsselrolle in vielen chemischen und biologischen Prozessen. In Science berichten Dahms et al. über die direkte Aufzeichnung ultraschneller Protonbewegungen mittels Schwingungsspektroskopie. Sie zeigen, dass Protonen in Wasser vorwiegend zwischen zwei Wassermolekülen gebunden sind und dort fluktuierende Bewegungen im Femtosekundenbereich ausführen. Diese Dynamik ist 10 bis 50 Mal schneller als das Hüpfen des Protons in eine neue Umgebung, der elementare Schritt der Protonenwanderung in der Chemie.
Das Proton, der positiv geladene Kern H+ des Wasserstoffatoms und kleinste chemische Einheit, spielt eine Schlüsselrolle in der Chemie und der Biologie. Säuren entlassen Protonen in eine wässrige Umgebung, in der sie hochbeweglich sind und den Transport elektrischer Ladung dominieren. In biologischen Systemen ist der Konzentrationsgradient von Protonen über Zellmembranen die treibende Kraft der Zellatmung und Energiespeicherung. Selbst nach Jahrzehnten intensiver Forschung sind jedoch die molekularen Geometrien des Protons in Wasser und die Elementarprozesse der Protonendynamik hoch kontrovers geblieben.
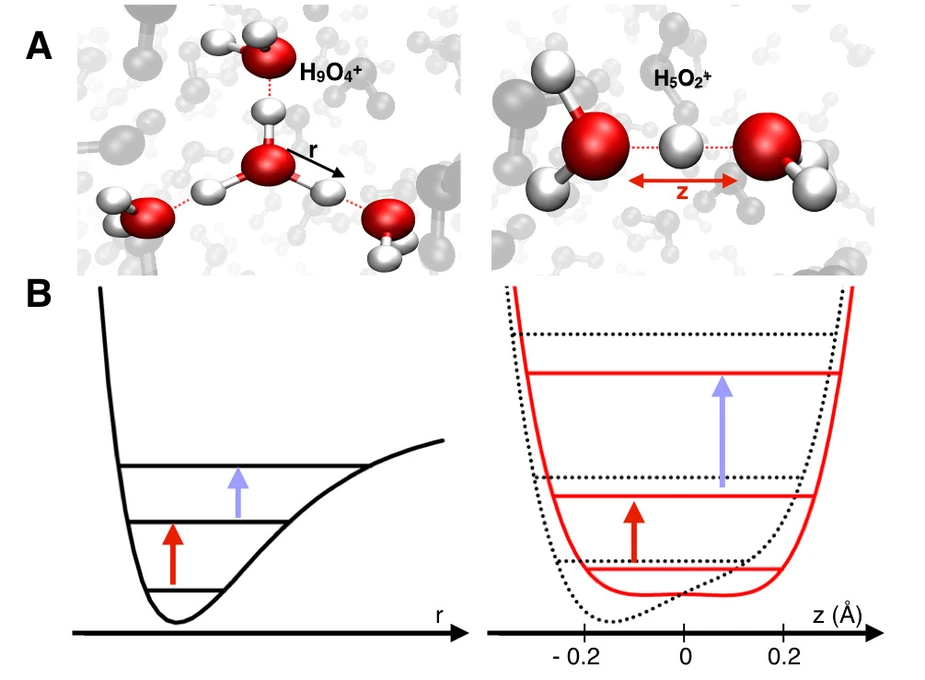
Protonen in Wasser werden üblicherweise durch die beiden in Abb. 1A gezeigten Grenzstrukturen beschrieben. Im sogenannten Eigen-Komplex (H9O4+) (links) ist das Proton Teil des zentralen H3O+-Moleküls, das von drei Wassermolekülen umgeben ist. Im Zundel-Kation (H5O2+) (rechts) bildet das Proton zwei starke Wasserstoffbrücken mit zwei benachbarten Wassermolekülen. Zur Beschreibung dieser Systeme auf molekularem Niveau wird die Energiepotentialfläche des Protons verwendet (Abb. 1B), die sich für die beiden Geometrien deutlich unterscheidet. Für den Eigenkomplex erwartet man ein anharmonisches Potential mit einem Minimum, während die Zundelgeometrie ein Doppelminimum-Potential aufweisen sollte. In Wasser sind solche Potentiale hochdynamisch und fluktuieren auf schnellen Zeitskalen, ein Verhalten, das durch thermische Bewegungen der umgebenden Wassermoleküle und des Protons verursacht wird.
Wissenschaftler des Max-Born-Instituts in Berlin und der Ben Gurion University of the Negev in Beer-Sheva, Israel, haben jetzt die ultraschnellen Bewegungen und transienten Strukturen von Protonen in Wasser unter Umgebungsbedingungen sichtbar gemacht. Sie berichten experimentelle und theoretische Ergebnisse in der Zeitschrift Science (doi:10.1126//science.aan5144), welche das Zundel-Kation als die in Wasser vorherrschende Spezies identifizieren. Die Femtosekundendynamik der Protonbewegungen (1 fs = 10-15 s) wurde mit Hilfe der Schwingungsübergänge zwischen den Quantenzuständen des Protons in Echtzeit aufgezeichnet (rote und blaue Pfeile in Abb. 1B). Die besonders aussagekräftige Methode der zweidimensionalen Schwingungsspektroskopie liefert die gelb-roten und blauen Konturen in Abb. 2A, die den Energiebereich der beiden Übergänge kennzeichnen. Die blaue Kontur befindet sich bei höheren Detektionsfrequenzen als die gelb-rote. Dieses Resultat stellt den ersten direkten Nachweis des Doppelminimum-Charakters des Protonpotentials (Abb. 1B rechts) in nativer wässriger Umgebung dar. Wäre das Proton in einem Potential mit einem Minimum gebunden (Abb. 1B links), würde die blaue Kontur bei kleineren Detektionsfrequenzen auftreten als die gelb-rote.
Die Ausrichtung beider Konturen entlang der vertikalen Frequenzachse zeigt, dass beide Schwingungsübergänge einen riesigen Frequenzbereich innerhalb von weniger als 100 fs durchlaufen. Dies ist eine direkte Folge der ultraschnellen Modulation der Potentialfläche durch die Umgebung. Mit anderen Worten: das Proton nimmt innerhalb von weniger als 100 fs vorübergehend alle Positionen zwischen den beiden Wassermolekülen ein und verliert extrem schnell die Erinnerung daran wo, es kurz vorher war. Die Modulation des Protonpotentials wird durch starke elektrische Felder verursacht, welche die Wassermoleküle der Umgebung auf das Zundel-Kation ausüben. Ihre schnelle thermische Bewegung führt zu starken Feldfluktuationen und Modulationen der Potentialfläche im Zeitbereich unter 100 fs. Dieses Bild wird unterstützt durch Referenzexperimente mit selektiv präparierten Zundel-Kationen in anderen Lösungsmitteln und durch detaillierte theoretische Simulationen der Protondynamik (Abb. 2B).
Ein Proton in einem einzelnem Zundel-Kation in Wasser wechselt in eine neue lokale Umgebung durch das Brechen und die Rekonstruktion von Wasserstoffbrücken. Diese Prozesse sind sehr viel langsamer als die Zitterbewegung des Protons und laufen im Zeitbereich einiger Pikosekunden ab (1 ps = 1000 fs = 10-12 s). Das hier vorgestellte neue Bild der Protondynamik ist von entscheidender Bedeutung für ein Verständnis des Protonentransports durch den berühmten von Grotthuss Mechanismus und für Protonverschiebungen in biologischen Systemen.
Originalpublikation:Science (2017) doi:10.1126//science.aan5144
Large-amplitude transfer motion of hydrated excess protons mapped by ultrafast 2D IR spectroscopy
Fabian Dahms, Benjamin P. Fingerhut, Erik T. J. Nibbering, Ehud Pines, Thomas Elsaesser
Abbildung 1: Chemische Struktur hydratisierter Protonen in Wasser.
A Schematische Darstellung des Eigen-Kations H9O4+ (links) und des Zundel-Kations H5O2+ (rechts). Die Pfeile markieren die Koordinate r der O-H Bindung und die (O...H+...O) Protontransfer-Koordinate z. Im Eigen-Kation wird das Proton durch eine kovalente O-H Bindung lokalisiert während es im Zundel-Kation zwischen den beiden Wassermolekülen delokalisiert ist.
B Anharmonisches Schwingungspotential (links) und Doppelminimumpotential des Zundel-Kations entlang der Koordinate z (rechts, rote Linie). Das Doppelminimumpotential wird durch die Einwirkung der Flüssigkeitsumgebung verzerrt (rechts, gepunktete Linie). Die roten und blauen Pfeile markieren Schwingungsübergänge zwischen den Quantenzuständen des Protons, rote Pfeile vom Grund- in den ersten angeregten Zustand und blaue Pfeile vom ersten in den zweiten angeregten Zustand. Eine Modulation der Potentialflächen verändert den Abstand der Quantenzustände und damit die Energie der Schwingungsübergänge was durch zweidimensionale Schwingungsspektroskopie nachgewiesen wird.
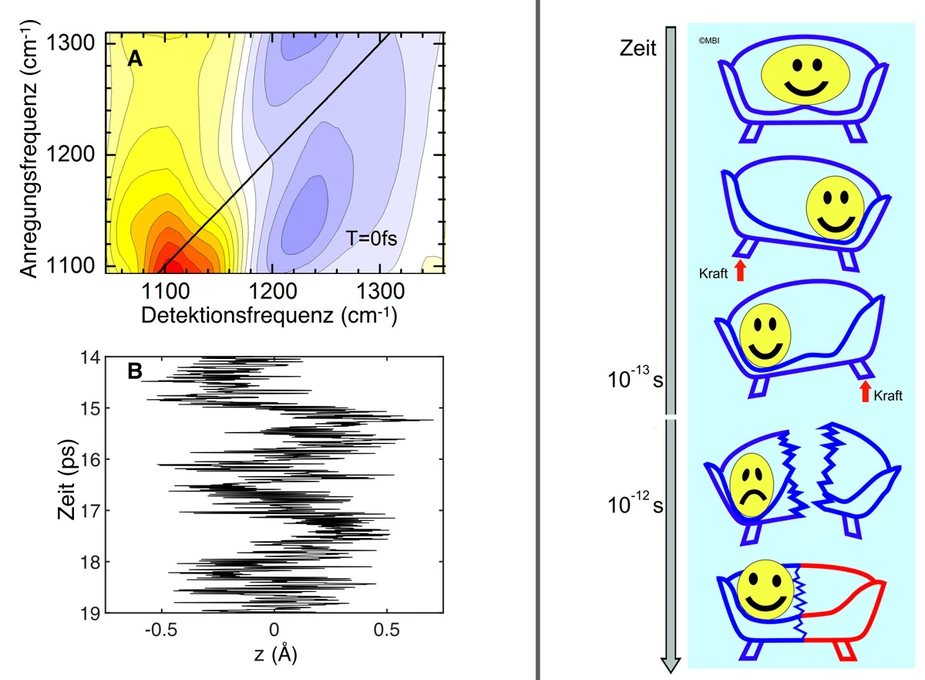
Abbildung 2: Femtosekundendynamik der Protonbewegung (1 fs = 10-15 s).
A Zweidimensionales Schwingungsspektrum mit dem Übergang vom Grund- in den ersten angeregten Zustand (gelb-rote Kontur) und vom ersten in den zweiten angeregten Zustand (blaue Kontur). Die Ausrichtung der beiden Konturen entlang der Achse der Anregungsfrequenz wird durch ultraschnelle Frequenzfluktuationen und den Gedächtnisverlust in der Protonposition verursacht.
B Theoretisch berechnete Echtzeitdynamik des Protons im Zundel-Kation. Innerhalb von weniger als 100 fs erfährt das Proton große Auslenkungen entlang der z-Koordinate, die die beiden Wassermoleküle verbindet. Auf Grund der ultraschnellen Modulation des Potentials durch die umgebenden Wassermoleküle nimmt das Proton vorübergehend alle Positionen entlang z ein.
Abbildung 3: Veranschaulichung der Dynamik hydratisierter Protonen in einem Bild der klassischen Physik.
Das Proton Smiley sitzt in der Mitte eines Sofas mit zwei Plätzen. Wenn das Sofa durch eine mechanische Kraft angehoben oder abgesenkt wird verändert sich die Form der Sitzfläche und das Proton bewegt sich auf dem Sofa hin und her. Diese Bewegungen treten im realen System auf einer Zeitskala unterhalb von 100 fs (10-13 s) auf. Nach einer Durchschnittszeit von ca. 1 ps = 1000 fs = 10-12 s zerbricht das Sofa und das Proton bewegt sich an einen neuen Platz. Das neue Sofa besteht aus einem Teil des alten (blau) und einem neuen Teil (rot).
Kontakt:
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie
Prof. Thomas Elsässer, elsasser(at)mbi-berlin.de, phone +49 30 6392-1400
Dr. Benjamin Fingerhut, fingerhut(at)mbi-berlin.de, phone +49 30 6392-1404
Dr. Erik T. J. Nibbering, nibberin(at)mbi-berlin.de, phone +49 30 6392-1477
Prof. E. Pines, epines(at)bgu.ac.il, phone +972 8 6461640