Magnesium-Ionen verlangsamen die Wasserdynamik auf kurzen Längenskalen
Experimente von MBI, FU Berlin und LMU München zeigen den Einfluss von Ionen auf die sie umgebenden Wassermoleküle
Die Anwesenheit von Ionen beeinflusst die Struktur und Dynamik von Wasser auf einer Vielzahl von Längen- und Zeitskalen. Neue Ergebnisse der Ultrakurzzeitspektroskopie und theoretische Analysen zeigen, dass die individuellen Wasserumgebungen spezifischer Paare von Magnesium- und Sulfat-Ionen prägend für die Dynamik wässriger Lösungen sind.
Flüssiges Wasser, das Ursprungsmedium für biochemische und zelluläre Prozesse, besteht aus einem komplexen Netzwerk polarer Moleküle, die durch Wasserstoffbrücken verbunden sind. Wasser reagiert auf das Vorhandensein eines gelösten Stoffes, indem es seine lokale Struktur verändert. Der Einfluss von negativ und positiv geladenen Ionen auf flüssiges Wasser wird üblicherweise anhand der Hofmeister-Reihe klassifiziert. Diese ordnet die Ionen anhand ihrer Eigenschaft, das sie umgebende Wasser zu strukturieren oder die Wasserstruktur aufzubrechen. Die mikroskopischen Ursachen und molekularen Mechanismen der Hoffmeister-Serie sind trotz langjähriger Forschung umstritten: Diese besitzt jedoch große Relevanz, da sie die Stärke des Einflusses von Ionen auf in Wasser gelöste Biomoleküle charakterisiert.
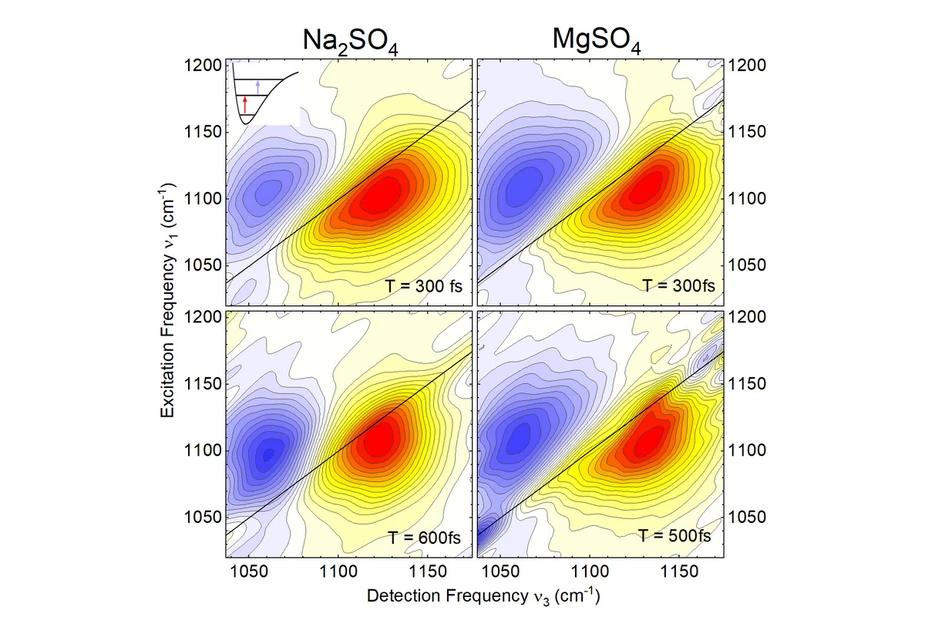
Neueste Experimente und Simulationen haben nun einen bedeutend komplexeren Einfluss von Ionen auf die sie umgebenden Wassermoleküle enthüllt. Die in der Zeitschrift „ACS Physical Chemistry Au“ publizierte Studie verbindet spektroskopische Experimente mit eingehenden theoretischen Analysen der molekularen Wechselwirkungen und der molekularen Dynamik. Hierbei benutzen die Forscher des Max-Born-Instituts in Berlin, der Freien Universität Berlin und der Ludwig-Maximilians-Universität München die asymmetrischen Steckschwingungen von Sulfat (SO42-)-Ionen als lokal sensitive Sonden, um die dynamischen Eigenschaften der Umgebung abzubilden. Hydratisierte Sulfat-Ionen stellen hierbei ein prototypisches Modellsystem dar, da diese häufig in Mineralien vorkommen und in der Physiologie und Biochemie von großer Bedeutung sind. Die Forscher verwendeten die experimentelle Technik der zweidimensionalen Infrarotspektroskopie im Femtosekunden-Zeitbereich, um das Verhalten der Sulfat-Ionen in Gegenwart von Natrium (Na+)- oder Magnesium (Mg2+)-Ionen bei geringen Ionenkonzentrationen zu vergleichen (Abbildung 1) und so Informationen über die Eigenschaften der lokalen Umgebung zu erhalten. Es zeigt sich, dass die Gegenwart von Mg2+-Ionen schnelle Fluktuationen der Wasserhülle um ein Sulfation reduziert und so zu einer spezifischen Verlangsamung der Solvatationsdynamik des hydratisierten MgSO4 im Vergleich zu wässrigen Na2SO4 Lösungen führt.
Abbildung 1: Zweidimensionale Infrarotspektren der asymmetrischen Streckschwingung des SO42--Ions für Natriumsulfat (Na2SO4, linke Spalte) und Magnesiumsulfat (MgSO4, rechte Spalte) in Wasser. Die Stärke der Schwingungsanregung ist in Abhängigkeit der Anregungsfrequenz ν1 und der Detektionsfrequenz ν3 aufgetragen. Gelb-rote Konturen entsprechen Anregungen des fundamentalen Schwingungsübergangs zwischen dem v=0 und 1 Zustand der Schwingung (roter Pfeil im Einsatzbild oben links), während blaue Konturen auf Obertonanregungen (v=1 nach 2, blauer Pfeil) zurückzuführen sind. Für Natriumsulfat wird eine Veränderung der rot-gelben Kontur von einer elliptischen Linienform (oben links) in eine mehr runde Form (unten links) innerhalb von ca. 300 fs beobachtet. Dies ist auf schnell fluktuierende Kräfte zurückzuführen, die die Wasserumgebung auf das Sulfation ausübt. Im Gegensatz zu diesem Verhalten bleibt für Magnesiumsulfat (rechte Spalte) die elliptische Linienform auf dieser Zeitskala erhalten. Hier werden schnelle Fluktuationen durch die Anwesenheit von Magnesium-Ionen in der unmittelbaren Nachbarschaft des Sulfations weitgehend unterdrückt.
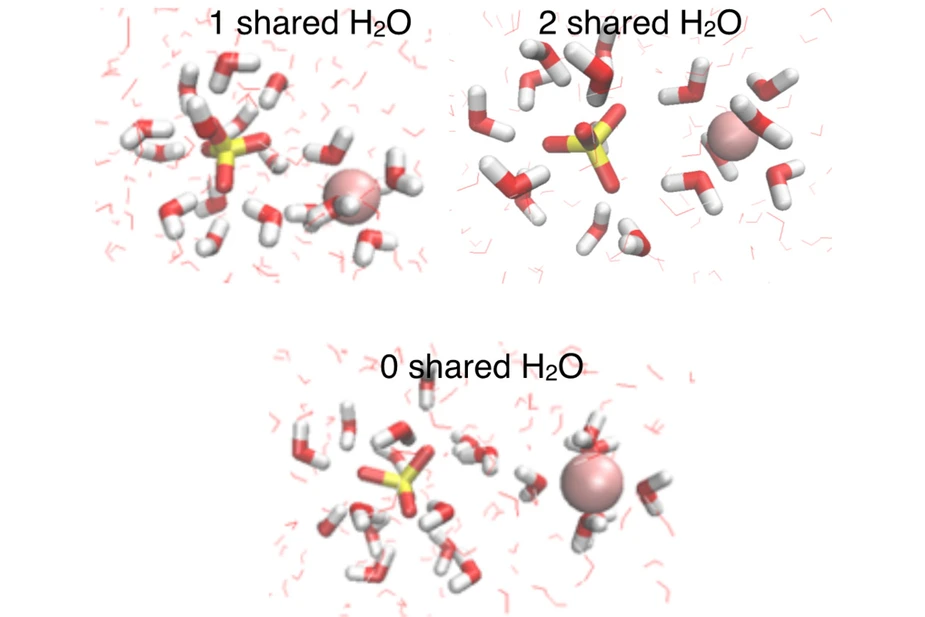
Umfangreiche Simulationen liefern eine mikroskopische Sicht auf die beobachtete Dynamik und zeigen ein molekulares Bild, bei dem die Verlangsamung der Wasserdynamik aus strukturellen Besonderheiten von SO42- - Mg2+-Ionenpaaren resultiert, die sich Wassermoleküle in ihrer Hydrathülle teilen (Abbildung 2). Die beschriebenen Effekte sind, im Gegensatz zur weitverbreiteten Darstellung in der Literatur, von kurzer Reichweite und beschränkt auf die ersten 1 bis 2 Wasserlagen um das Sulfation. Im Gegensatz zur Hoffmeister-Reihe, welche die Wirkung von Ionentypen auf die Wasserstruktur klassifiziert, zeigen die Ergebnisse die besondere Bedeutung individueller Solvatationsgeometrien spezifischer Ionenpaare, welche prägend sind für die Dynamik verdünnter wässriger Systeme.
Abbildung 2: Strukturelle Darstellung von Mg2+- SO42- Ionenpaaren in wässriger Lösung. Die Simulationen zeigen ein molekulares Bild, bei dem die Verlangsamung der Hydratationsdynamik aus strukturellen Besonderheiten von SO42- - Mg2+ Ionenpaaren resultiert, die sich 1 oder 2 Wassermoleküle in ihrer Hydrathülle teilen (oben), wogegen Ionenpaare mit separaten, vollständigen Hydrathüllen (unten) nur geringen Einfluss auf die Wasserdynamik haben. Schwefelatome sind gelb, Magnesiumatome pink, Sauerstoffatome rot und Wasserstoffatome weiß dargestellt; Wassermoleküle in den ersten Hydratationsschalen um die Ionen sind hervorgehoben.
Publikation
Short-Range Cooperative Slow-down of Water Solvation Dynamics Around SO42−−Mg2+ Ion Pairs.
Achintya Kundu, Shavkat I. Mamatkulov, Florian N. Brünig, Douwe Jan Bonthuis, Roland R. Netz, Thomas Elsaesser, and Benjamin P. Fingerhut
ACS Physical Chemistry Au (open access, ACS Editor’s Choice) (2022), doi: 10.1021/acsphyschemau.2c00034, https://pubs.acs.org/doi/full/10.1021/acsphyschemau.2c00034
Kontakt
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie (MBI)
Dr. Achintya Kundu
Tel. +49 30 6392-1414
E-Mail Achintya.Kundu(at)mbi-berlin.de
Prof. Dr. Thomas Elsässer
Tel. +49 30 6392-1400
E-Mail Thomas.Elsaesser(at)mbi-berlin.de
Forschungsverbund Berlin e.V.
Anja Wirsing
Pressereferentin
Tel. +49 30 6392-3337
wirsing(at)fv-berlin.de
Pressemitteilung MBI vom 12.10.2022